一、纯水的质量要求、检验及制备方法
分析实验室对纯水的质量要求应该根据工作性质而定,不能一概而论。理论纯水的电导率是0. 0548μS/cm(25°C ),若用电阻率表示是18. 3MΩ • cm(25°C)。分析实验室对纯水的质量要求达到最高也只能接近理论纯水的电导率,实际上很难达到,因为它要求实验室使用的盛水容器、管路等设备的清洁程度也必须处于理想状态。实际上,分析实验室对纯水质量要求可分为三个档次,即一级纯水、二级纯水和三级纯水。一级纯水用于制备标准水样或超痕量物质分析,二级纯水用于精确分析和研究工作,三级纯水适用于一般实验室工作。
(1)纯水的质量指标
纯水的质量指标主要是用pH值、电导率、可氧化物限度、吸光度和二氧化硅的含量来表示,它主要反映了纯水中无机离子、还原性物质和尘埃粒子的含量水平,将纯水的级别与质量指标对照应符合表1的范围。
| 指标名称 | 一级纯水 | 二级纯水 | 三级纯水 |
| pH值范围(25℃) | 6. 8〜7. 2 | 6. 6 〜7. 2 | 5.0 〜7. 5 |
| 电导率(25*C)/(μS/cm) | ≤0. 1 | ≤1.0 | ≤5. 0 |
| 电阻率(25r)/(MQ·cm) | ≥10 | ≥1 | ≥0. 2 |
| 吸光度(254nm.lcm光程) | ≤0. 001 | ≤0. 01 | — |
| 二氧化硅/(mg/L) | ≤0. 02 | ≤0. 05 | — |
| 可氧化物的限度试验(KMnO4保持颜色的最低时间)/min | 60 | 60 | 10 |
表1纯水的级别与质量指标
(2)纯水的质量检验
分析实验过程中会大量使用纯水,水的纯度对分析结果的空白值起到至关重要的作用,将直接关系实验的成功与失败,因此,必须定期检查纯水的质量。
①电导率的测定电导率是纯水质量的一个重要指标,实验室中用电导仪进行测量纯水电导率的大小,用以判断水的纯度和级别。
在不同温度下,测量同一纯水的电导率结果是不同的,即电导率受温度影响。目前市场销售的电导仪一般具有温度补偿装置,根据仪器说明书操作规定,测量纯水的电导率。如果所用的电导仪不具备温度补偿功能,则可先在室内温度下测定t℃的电导率,然后用下面的公式计算25°C的电导率。
K25=a(Kt-Kp)+0. 0548
上式中,K25为25°C时的纯水电导率,μS/cm;a为t(°C)时换算系数;Kt为t(°C)时实测的纯水电导率,μS/cm; Kp为t(°C)时理论纯水电导率,μS/cm;0.0548为25°C时理论纯水电导率,μS/cm。
上式中,不同温度时的换算系数a和理论纯水电导率是不同的,见表2。
|
t/°C |
a |
Kp/(μS/cm) |
Z/°C |
a |
Kp/(μS/cm) |
|
0 |
1. 873 |
0. 0111 |
20 |
1. 111 |
0.0414 |
|
5 |
1. 6251 |
0. 0160 |
25 |
1. 000 |
0. 0548 |
|
10 |
1.413 |
0. 0224 |
30 |
0. 903 |
0. 0710 |
|
15 |
1. 250 |
0. 0308 |
35 |
0. 822 |
0. 0908 |
表2 电导率的换算系数a和理论纯水电导率Kp与温度t(℃)的关系
②pH值测定 纯水精密的pH值可以采用pH计进行测定,粗略的pH值可以采用精密pH试纸进行检查,纯水的pH值一般在6. 5-7. 5之间。
③吸光度测定用紫外分光光度计测定纯水的吸光度。选用波长为254nm,光程为1cm的比色皿进行测定,测得结果后,以纯水质量指标来判断级别。
④可溶性二氧化硅的测定 按GB 6682—1986中“2. 5二氧化硅的测定"操作规程进行。
⑤可氧化物检验即是检验纯水中的还原性物质的含量,一般采用还原高镒酸钾的能力程度表明纯水中还原性物质的含量。可按如下操作进行检验:取1000mL二级水(100mL三级水)注入烧杯中,加入10.0mL硫酸溶液(按GB625—1977配制,约98g/L)和1.0mL高锭酸钾溶液(按GB 643—1977配制,浓度为0.01mol/L新鲜溶液)盖上表面皿,煮沸5min, 与置于另一相同容器中不加试剂的等体积水样对照,溶液的淡红色不得完全褪色。
上面叙述的纯水质量检验,在农业环境监测系统实验室中无需各项均做例行检验,一般只需定期地进行纯水的电导率测定即可。
(3)纯水的制备方法
制备纯水的方法很多,通常采用以下4种方法,即蒸馏法、离子交换法、亚沸蒸馏法和电渗析法。
①蒸馏法 蒸馏法制备纯水是利用杂质与水的沸点不同,杂质与水蒸气不能一同蒸发而达到分离水中杂质的目的。
水中杂质分为挥发性和不挥发性两类。不挥发性杂质,包括大多数无机盐、碱和某些有机化合物。这类杂质用蒸馏法很容易除去。而对于水中的挥发性杂质,如溶解在水的气体、多种酸、有机物及某些盐的分解产物也会随水蒸气蒸循出进入馏出液而无法分离。
解决分离挥发性杂质的办法,是在水中加入一些试剂,使杂质的挥发性转变为不挥发性。例如,在水中加入高镒酸钾,可将有机物氧化成二氧化碳和水,达到除去有机物的目的。为了除去水中挥发性酸和溶解在水中的酸性气体,可以通过加入碱性物质与水中的酸性物质在蒸馏前化合。此类的碱性物质可使用氧化锐、过氧化钠等,可中和水中的硝酸、二氧化碳和硫化氢等酸物质,达到分离此类挥发性的酸类物质。此外,水中存在氨和胺类物质可加入铭酸酎或磷酸酊与之化合,通过蒸馏达到分离。
在分析实验室中,用蒸馏法制备纯水通常采用以下两类蒸馏器:硬质化学玻璃制成的蒸馏器和石英蒸馏器。使用铜或其他金属制成的蒸馏器,蒸得的蒸馏水中所含的金属杂质,例如铜、锡等,其浓度往往高于原水。不适用于痕量元素的分析。使用硬质化学玻璃制成的蒸馏器所得到蒸馅水比较纯净,适用于常规用途。由于硬质化学玻璃中含有一定数量的硼,故所得的蒸馏水不适用于硼的测量。石英蒸馏器所得到蒸馏水更为纯净,适合于一般实验室痕量元素的分析工作。但是石英蒸馏器价格昂贵,蒸馏瓶体积比较小,出水率比较低,适合科研和少量样品的分析测试用水,若样品数量多,用水数量大则无法适应。
亚沸蒸馏水适合制备高纯水。近年来出现的一种新型石英亚沸蒸馏器,其加热方式是将电阻丝封闭在石英管中置于液面上方的间接加热。其特点是在液面上方加热,使液面始终处于亚沸状态,可使水蒸气带出的杂质降至最低。该装置还适用于制备高纯酸(如HCI、HNO3)和氨水。
亚沸蒸馏水另外一种加热方式是光加热。以灯光作热源,照射液体表面,水从液面气化蒸发,可避免沸腾时携带或沿表面蠕升的现象发生,蒸得的水极纯,可称为高纯水。
②离子交换法用离子交换法制备的纯水称为去离子水。用离子交换法制备纯水的优点是设备简单、操作简便、出水量大、成本低,非常适合于用水量大的分析实验室。用离子交换法可除去水中绝大部分的盐类、碱和游离酸,但不能完全除去有机物和非电解质。去离子水适用于测定无机微量元素而不太适合用于有机分析。若要获得既无无机类杂质又无有机类杂质的纯水,可将离子交换水再蒸馏一次。建议离子交换使用的原水采用市售的蒸馏水或电渗析水,这对提高水的纯度和减少树脂再生处理次数、提高树脂利用率均是有利的。
1)离子交换法的原理。离子交换法制备去离子水的基本原理是利用阳、阴离子交换树脂上的可交换的H+和OH-与水中其他的阳离子和阴离子的交换作用,将水中的离子除去而达到制备水的目的。离子交换反应如下:
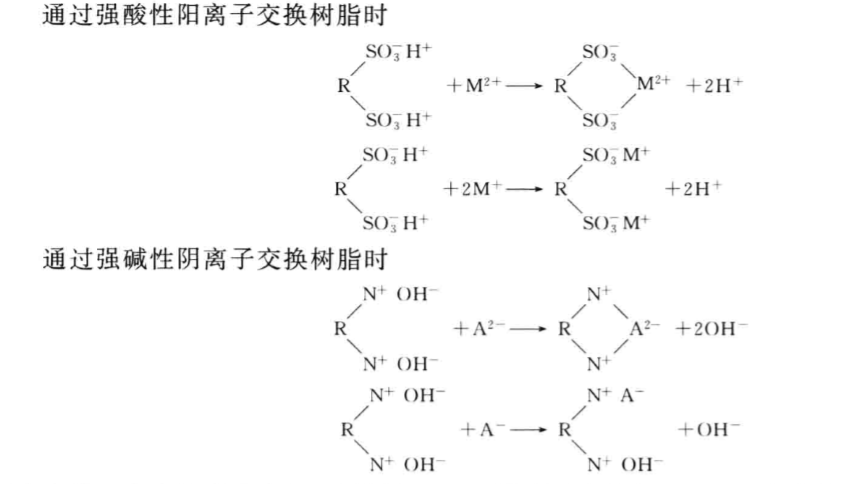
两次交换,水中阳离子交换了树脂上H+阴离子交换了OH-,水中的阳、阴离子交换到树脂上,而由树脂上交换下来等量的H+和OH-结合成水,达到了纯化水的目的。
2)树脂的选择、处理、装柱和淋洗。用离子交换法制取纯水,一般采用的是强酸型阳离子交换树脂和强碱型阴离子交换树脂。树脂上可交换的离子应是氢型和氢氧型,如果是钠型和氯型,应加以处理转为氢型和氢氧型后才能使用。